VÍRUS DA PARAINFLUENZA 1/2/3, INFECÇÃO POR – RT-QPCR QUALITATIVO [cód. 12518]
NOME DO EXAME
Vírus da Parainfluenza 1 / 2 / 3
OUTROS NOMES DO EXAME
HPIV-1; HPIV-2; HPIV-3; HPIV-4; Teste do vírus da parainfluenza humana; Teste HPIV; Teste HPIV-1; Teste HPIV-2, teste HPIV-3; Paraflu 1-4 PCR; Parainfluenza 1-4 por PCR; Painel de PCR parainfluenza; PIV
UTILIDADE DO EXAME
Os testes de PCR para parainfluenza são úteis para o diagnóstico rápido e preciso de infecções pelo vírus parainfluenza orientando o tratamento adequado e as medidas de controle de infecção.
TIPO DE ESPÉCIME
Obtenção de amostras Swab Nasal ou Escarro. Exame exclusivamente para pacientes com sintomatologia.
INFORMAÇÃO NECESSÁRIA
A amostra para exame pode ser coletado no domicílio sem qualquer custo adicional. Os prazos para entrega de resultados obedecem aos seguintes critérios: Amostras coletadas no domicílio (preferível) das 7 às 12 horas terão laudos emitidos até as 18 horas do mesmo dia. Amostras coletadas no domicílio entre 13 e 24 horas terão laudos emitidos até as 7 h do dia seguinte.
INSTRUÇÕES DE ENVIO
Conservação para transporte em São Paulo a temperatura ambiente (estável por 48 horas).
AMOSTRAS REJEITADAS
Amostras enviadas sem meio de transporte viral .
Aliquotagem de amostras para exames moleculares
Alíquota refere-se a uma parte ou porção representativa de uma amostra maior, que é separada para ser utilizada em outro experimento.
Para que nenhuma informação seja perdida nesse processo, o laboratório deve manter um controle de alíquotas e, em um primeiro momento, o técnico identifica o microtubo que receberá a alíquota e, ao mesmo tempo, a registra no sistema. A alíquota deve ser realizada por um técnico de laboratório familiarizado com os objetivos e os resultados esperados.
O exemplo de aliquotagem será do líquido de Citologia de Base Líquida (CBL). A CBL, também conhecida como citologia oncótica em meio líquido ou citologia em meio líquido, é uma técnica onde, ao invés de raspagens na lâmina, as células são coletadas e suspensas em um líquido preservante com metanol, que é tóxico, requerendo uso de luvas.
O líquido da CBL pode conter células livres, debris, células inflamatórias, hemácias, bactérias, vírus, fungos, protozoários, DNA livre, espermatozoides, fibrina, resíduos de cremes, outras substâncias usadas na lavagem vaginal, e mais. Essas partículas estão parcialmente livres no líquido ou sedimentadas no fundo, e o exame de Patologia Molecular busca extrair todo o DNA e RNA presentes na amostra.
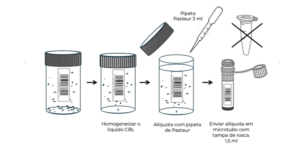
O técnico deve homogeneizar a amostra para que tudo seja representado, submetendo-a a forte agitação motora. Em seguida, transferir 1,5 ml desse líquido usando uma pipeta de Pasteur para o microtubo e descartá-lo. Usar um microtubo com tampa de rosca (Kasvi é recomendado) e nunca um microtubo de fechamento por pressão, pois este pode abrir espontaneamente no traslado ao laboratório. Lembre-se: se aliquotar mais do que o necessário (CBL originalmente contém 18 ml de preservante), pode-se interferir no processamento automático da citologia por pouco líquido. Nestes casos, o técnico deverá repor o volume com líquido preservante ou, na falta deste, com álcool 70%.
Medidas para aliquotagem abaixo. Dica: se enviar ≥ 4 ml, utilize um tubo Falcon (ou similar) de 15 ml, como na figura ao lado. PCR para HPV – 2 ml
PCR para HPV – 2 ml
PCR para Painel Ginecológico – 2 ml
PCR para HPV e Painel Ginecológico – 2 ml
Captura Hibrida HPV – 4 ml
Captura para HPV + PCR para HPV – 6 ml
Captura para HPV + PCR para painel ginecológico – 6 ml
Captura para HPV + PCR para HPV e painel ginecológico – 6 ml.
METODOLOGIA
Detecção baseado em Tecnologia do PCR em tempo real (RT-PCR). Os vírus são detectados com primers de sonda Taqman da Thermo Fisher®. Os ensaios moleculares multiplex, que dependem da detecção de ácidos nucleicos virais, fornecem resultados rápidos com alta sensibilidade e especificidade, tornando-os testes ideais quando usados no contexto de uma avaliação clínica cuidadosa.
PRAZO
Até 6 horas
INFORMAÇÃO CLÍNICA
Os vírus da parainfluenza humana (HPIVs) são vírus de RNA não segmentados que pertencem aos gêneros Paramyxovirus (HPIV tipo 1 [HPIV-1] e HPIV-3) e Rubulavirus (HPIV-2 e HPIV-4) da família Paramyxoviridae. O HPIV-4 é dividido em dois subtipos, subtipos A e B, com base nas diferenças antigênicas. Os HPIV-1, -2 e -3 são patógenos respiratórios importantes e são as principais causas de crupe, bronquiolite e pneumonia em bebês e crianças pequenas. Eles foram estimados como a causa de 40% das doenças agudas do trato respiratório em crianças das quais um vírus é recuperável e 20% das doenças respiratórias em crianças hospitalizadas. O HPIV-4 tem sido tradicionalmente associado a infecções leves do trato respiratório superior em crianças e adultos.
O diagnóstico etiológico de infecções por HPIV não pode ser baseado exclusivamente em sinais e sintomas clínicos porque outros patógenos causam síndromes semelhantes. O uso de métodos diagnósticos clássicos, como isolamento viral e sorologia, pode resultar em atrasos de várias semanas antes que os resultados dos testes estejam disponíveis. O diagnóstico rápido é desejável tanto para auxiliar o clínico na tomada de decisões terapêuticas quanto para prevenir infecções nosocomiais baseia-se em técnicas moleculares de transcrição reversa (RT)-PCR o que constitui uma abordagem para diagnóstico rápido com esperada alta sensibilidade.
Utilizamos o método primer-sonda para detecções de fragmentos do DNA/RNA virais em equipamentos de PCR em tempo real (RT-qPCR ou transcriptase reversa qualitativa e quantitativa PCR). Logo, este método de detecção é direto. A tabela 1 apresenta as informações dos protocolos de amplificação utilizados assim como a comparação deles com alguns kits comerciais.
INTERPRETAÇÕES
Os vírus e respectivas regiões-alvos de seus genomas estão descritos na primeira e segunda colunas, respectivamente. Os limites de detecção apresentados na terceira coluna foram estimados através da diluição seriada dos genomas virais, sendo consideradas os menores números de cópias para os quais 100% das reações foram positivas. As porcentagens de concordâncias dos resultados positivos e negativos obtidos com nosso protocolo e outros protocolos comerciais estão apresentados na quarta e na quinta colunas, respectivamente.
Tabela 1. Protocolo de detecção dos vírus respiratórios.
![]()
Observações: Resultados obtidos na comparação com o ensaio RespiFinder‐2Smart (PathoFinder)
Interpretação do Exame
1. Resultado “Detectado” indica a presença do patógeno na amostra.
2. Resultado “Não Detectado” indica a ausência do patógeno ou concentração inferior ao limite de detecção (LoD) do teste.
3. Resultado “Inconclusivo”: Sem amplificação do controle interno.
Nem todos os resultados positivos indicam infecção ativa atual. Episódios assintomáticos são especialmente comuns para bocavírus e rinovírus, então um julgamento clínico deve ser feito sobre se o vírus detectado está causando os sintomas do paciente ou se os sintomas estão ocorrendo incidentalmente durante um período de detecção viral assintomática.
Estabilidade
Refrigerada: 2º a 8ºC até 72 horas

Genoa e Encodexa são duas marcas LPCM
