HAEMOPHILUS DUCREYI (CANCRO MOLE) PESQUISA DO DNA, PCR [cód. 12771]
NOME DO EXAME
Haemophilus Ducreyi
OUTROS NOMES DO EXAME
Haemophilus Ducreyi; Cancro Mole; Úlcera Mole; Cancroide; Cancro de Ducreyi; Cancroide Bubão; Ferida Mole;
UTILIDADE DO EXAME
Este teste deve ser solicitado pelo médico e objetiva: Prevenir complicações. A Haemophilus Ducreyi não tratada pode se espalhar e levar a complicações graves ou sequelas em ambos os sexos; Prevenir a transmissão para parceiros sexuais; Muitas pessoas com Haemophilus Ducreyi não apresentam sintomas mas são capazes de transmitir.
NECESSIDADE DE PEDIDO MÉDICO
O pedido médico deve ser enviado juntamente com a amostra.
COBERTURA OPERADORA PLANO DE SAÚDE
Os planos de saúde não cobrem a pesquisa molecular de Haemophilus ducreyi
NECESSIDADE DE CONSENTIMENTO
Não.
PREPARAÇÃO DA PACIENTE
Não há preparo
AMOSTRA
Swab de secreções de lesões ulceradas de vagina e pênis
INSTRUÇÕES DE COLETA E ARMAZENAMENTO DA AMOSTRA
A Genoa/LPCM fornece o “kit de coleta” necessário para a coleta da amostra vaginal, cervical e
anal.
ESTABILIDADE DA AMOSTRA
As secreções coletadas e armazenadas no líquido conservante são estáveis à temperatura
ambiente por até 3 dias.
VOLUME MÍNIMO DA AMOSTRA
O frasco fornecido contém 18 ml de solução conservante e pode ser utilizado para análise citológica e pesquisa de agentes infecciosos, incluindo Haemophilus Ducreyi.
RETENÇÃO DA AMOSTRA
O tempo de retenção da amostra pelo laboratório fixada é de 10 dias.
Aliquotagem de amostras para exames moleculares
Alíquota refere-se a uma parte ou porção representativa de uma amostra maior, que é separada para ser utilizada em outro experimento.
Para que nenhuma informação seja perdida nesse processo, o laboratório deve manter um controle de alíquotas e, em um primeiro momento, o técnico identifica o microtubo que receberá a alíquota e, ao mesmo tempo, a registra no sistema. A alíquota deve ser realizada por um técnico de laboratório familiarizado com os objetivos e os resultados esperados.
O exemplo de aliquotagem será do líquido de Citologia de Base Líquida (CBL). A CBL, também conhecida como citologia oncótica em meio líquido ou citologia em meio líquido, é uma técnica onde, ao invés de raspagens na lâmina, as células são coletadas e suspensas em um líquido preservante com metanol, que é tóxico, requerendo uso de luvas.
O líquido da CBL pode conter células livres, debris, células inflamatórias, hemácias, bactérias, vírus, fungos, protozoários, DNA livre, espermatozoides, fibrina, resíduos de cremes, outras substâncias usadas na lavagem vaginal, e mais. Essas partículas estão parcialmente livres no líquido ou sedimentadas no fundo, e o exame de Patologia Molecular busca extrair todo o DNA e RNA presentes na amostra.
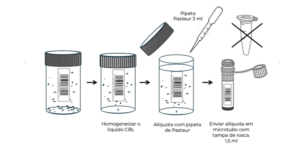
O técnico deve homogeneizar a amostra para que tudo seja representado, submetendo-a a forte agitação motora. Em seguida, transferir 1,5 ml desse líquido usando uma pipeta de Pasteur para o microtubo e descartá-lo. Usar um microtubo com tampa de rosca (Kasvi é recomendado) e nunca um microtubo de fechamento por pressão, pois este pode abrir espontaneamente no traslado ao laboratório. Lembre-se: se aliquotar mais do que o necessário (CBL originalmente contém 18 ml de preservante), pode-se interferir no processamento automático da citologia por pouco líquido. Nestes casos, o técnico deverá repor o volume com líquido preservante ou, na falta deste, com álcool 70%.
Medidas para aliquotagem abaixo. Dica: se enviar ≥ 4 ml, utilize um tubo Falcon (ou similar) de 15 ml, como na figura ao lado. PCR para HPV – 2 ml
PCR para HPV – 2 ml
PCR para Painel Ginecológico – 2 ml
PCR para HPV e Painel Ginecológico – 2 ml
Captura Hibrida HPV – 4 ml
Captura para HPV + PCR para HPV – 6 ml
Captura para HPV + PCR para painel ginecológico – 6 ml
Captura para HPV + PCR para HPV e painel ginecológico – 6 ml.
DESCRIÇÃO DA METODOLOGIA
A reação em cadeia da polimerase (abreviada PCR) é uma técnica de laboratório para produzir (amplificar) rapidamente milhões a bilhões de cópias de um segmento específico de DNA, que pode então ser estudado em maiores detalhes. A PCR envolve o uso de pequenos fragmentos sintéticos de DNA chamados primers para selecionar um segmento do genoma a ser amplificado, e então múltiplas rodadas de síntese de DNA para amplificar esse segmento.
SENSIBILIDADE
A sensibilidade do protocolo é elevada (>95%).
INFORMAÇÃO CLÍNICA
O cancroide é uma doença rara e os desafios para entender sua verdadeira incidência global são baseados em dificuldades em isolar o agente causador e as limitadas modalidades de diagnóstico e vigilância disponíveis para o clínico. O cancroide também foi considerado um cofator significativo na aquisição heterossexual e transmissão da doença do HIV. Úlceras genitais podem aumentar o risco de infecção pelo HIV em até 50 a 300 vezes por cada encontro desprotegido de relação sexual vaginal. A doença do HIV, por sua vez, pode alterar a aparência e o curso clínico do cancroide. Isso pode incluir um aumento no período de incubação, múltiplas lesões ulcerativas, atrasos na cura e resposta ruim a cursos padrão de antibióticos ou falhas no tratamento. O cancroide afeta predominantemente indivíduos sexualmente ativos mais jovens na faixa etária de 21 a 30 anos. Esse grupo reflete uma grande proporção de profissionais do sexo e a típica população masculina mais jovem em países em desenvolvimento que participam de seus serviços. Um estado de portador assintomático foi observado entre mulheres, potencialmente permitindo a transmissão insuspeita da doença.
A combinação de uma ou mais úlceras genitais profundas e dolorosas e adenopatia inguinal supurativa sensível indica o diagnóstico de cancroide; a linfadenite inguinal geralmente ocorre em <50% dos casos. Para fins clínicos e de vigilância, um diagnóstico provável de cancroide pode ser feito se todos os quatro critérios a seguir forem atendidos: 1) o paciente tem uma ou mais úlceras genitais dolorosas; 2) a apresentação clínica, a aparência de úlceras genitais e, se presente, linfadenopatia regional são típicas de cancroide; 3) o paciente não tem evidência de infecção por Treponema pallidum por exame de campo escuro ou NAAT (ou seja, exsudato da úlcera ou fluido seroso) ou por testes sorológicos para sífilis realizados pelo menos 7 a 14 dias após o início das úlceras; e 4) o NAAT para Vírus Herpes Simplex 1 ou 2, ou a cultura para HSV realizada no exsudato ou fluido da úlcera são negativos.
Um diagnóstico definitivo de cancroide requer a identificação de H. ducreyi em meios de cultura especiais que não estão amplamente disponíveis em fontes comerciais; mesmo quando esses meios são usados, a sensibilidade é <80%. O NAAT (Teste de Amplificação de Ácido Nucleico), especificamente PCR, é um método promissor e potencialmente superior para detecção rápida de Haemophilus ducreyi (cancroide) em comparação aos métodos de cultura tradicionais,
RESULTADO E INTERPRETAÇÃO
O resultado é apresentado de forma simples e objetiva, a fim de facilitar sua compreensão. Contudo, a interpretação deste resultado é um ato médico e deve ser realizada levando-se em consideração os dados clínicos e demais exames do paciente.
Os três resultados possíveis e suas interpretações estão apresentados a seguir.
Detectado – este resultado indica que Treponema pallidum é detectada na amostra analisada.
Não Detectado – este resultado indica que Treponema pallidum está ausente ou abaixo dos limites de deteção do método na amostra analisada.
Celularidade Abaixo do Detectável – este resultado indica que não é possível obter DNA com a qualidade e/ou em quantidade necessárias para a realização do exame. Alternativamente, inibidores de reação (por exemplo, lubrificantes) podem estar presentes e interferi nas reações enzimática, impedindo a realização do exame.
DISPONIBILIDADE DO LAUDO (TAT)
O laudo estará disponível 3 a 5 dias úteis após a autorização do exame.
VALORES DE REFERÊNCIA
Negativo. Os valores de referência se aplicam a todas as idades.
PRECAUÇÕES
Fatores como coleta inadequada da amostra, tipo de amostra biológica, tempo decorrido entre a coleta e o início dos sintomas e oscilação da quantidade da bactéria podem influenciar no resultado do exame. Variações nas sequências dos DNA dos agentes infecciosos onde se anelam os primers podem gerar resultados falso-negativos. Havendo discordância entre o resultado do teste e o quadro clínico do paciente, aconselha-se que o exame seja repetido em outra amostra.
NOTAS
Este exame é desenvolvido e validado nos laboratórios da Genoa/LPCM.
OBSERVAÇÕES
A Encondexa está comprometida em manter a confidencialidade das informações dos pacientes. Volume Mínimo (quantidade de espécime necessária para realizar um ensaio uma vez.
Recepção do volume mínimo torna impossível repetir o teste ou realizar testes de confirmação. Em algumas situações, um volume mínimo do espécime pode resultar em quantidade não suficiente, exigindo que um segundo espécime seja coletado).
Informe se o caso envolve “Resultados Semi-Urgentes” definidos como resultados relacionados a doenças infecciosas prontamente necessários para evitar consequências de saúde potencialmente sérias para o paciente.
Teste URGENTE: em raras circunstâncias, o teste URGENTE do laboratório de referência pode ser necessário para pacientes que precisam de tratamento imediato. Para agendar o teste URGENTE, peça ao patologista, médico ou gestor de laboratório ou Representante para ligar para a Encodexa™ e uma vez acordado que há necessidade da categoria de teste URGENTE, serão feitos arranjos para atribuir recursos para executar o teste em uma base URGENTE quando a amostra for recebida.
A Encodexa™ usa no mínimo dois identificadores específicos do paciente para verificar se o paciente correto é correspondido com o espécime correto e o pedido correto para serviços de teste. Conforme um espécime é recebido na ENCODEXA, o nome e sobrenome do paciente, data de nascimento, número do prontuário médico e número de acesso do cliente são verificados comparando os rótulos no tubo ou recipiente do espécime com o pedido eletrônico e qualquer papelada (folha de lote ou formulário) que possa acompanhar o espécime a ser testado. Quando discrepâncias são identificadas, o Centro de Atendimento de Consultas da Encondexa telefonará para o cliente para verificar as informações discrepantes para garantir que a Encodexa™ esteja realizando o teste correto para o paciente correto. Os espécimes são considerados rotulados incorretamente quando há uma incompatibilidade entre os identificadores específicos da pessoa no espécime e as informações que acompanham o espécime. Quando identificação insuficiente ou inconsistente for enviada, a Encodexa™ recomendará que um novo espécime seja obtido.
Prazo dos exames (TAT) O extenso menu de testes do Encodexa™ reflete as necessidades de nossa própria prática de assistência médica. Estamos comprometidos em fornecer o TAT mais rápido possível para melhorar o diagnóstico e o tratamento. Consideramos os serviços laboratoriais como parte do continuum de atendimento ao paciente, em que as necessidades do paciente são primordiais. Nesse contexto, nos esforçamos para cumprir nossas obrigações de serviço. Nosso histórico de serviço e nossas métricas de qualidade documentarão nossa capacidade de entregar em todas as áreas de serviço, incluindo TAT. A Encodexa™ define TAT como o tempo de teste analítico (o tempo do qual uma amostra é recebida no local de teste até o momento do resultado) necessário e é listado para cada teste como “Relatório disponível”. O TAT é monitorado continuamente por cada local de laboratório em execução dentro da Encodexa™.

Genoa e Encodexa são duas marcas LPCM
